Em 19 de dezembro de 2023, a Igenesis anunciou que seu desenvolvimento independenteKit de diagnóstico para detecção de 16 vírus de alto risco e genotipagem de 16 e 18 papilomavírus humano (HPV) (método de sonda de fluorescência PCR) foi aprovado pelo Ministério da Saúde Pública da Tailândia após revisão rigorosa.O reagente obteve a certificação de registro TFDA de dispositivos médicos na Tailândia, o que o qualifica para entrar no mercado tailandês de dispositivos médicos e contribuir para a indústria local de construção médica e de saúde.Esta é outra boa notícia para a Igenesis, após o certificado de registro de dispositivo médico tailandês obtido por seu sistema qPCR automatizado totalmente fechado - Galaxy Nano e Galaxy Lite, reagente de detecção de ácido nucleico TB e kit de extração e purificação de ácido nucleico.
Segundo a Organização Mundial da Saúde (OMS), o câncer do colo do útero é o terceiro tipo de câncer mais comum entre as mulheres em todo o mundo, com uma taxa de incidência apenas inferior à do câncer de pulmão e de mama.Aproximadamente 600.000 mulheres são diagnosticadas com cancro do colo do útero todos os anos em todo o mundo, e cerca de 340.000 delas morrem desta doença.
Em 17 de novembro de 2020, a Organização Mundial da Saúde (OMS) lançou a Estratégia Global para Acelerar a Eliminação do Câncer Cervical, enfatizando a importância do teste e rastreamento do HPV.Em 6 de julho de 2021, a OMS atualizou e divulgou o documento “Prevenção do Câncer Cervical: Diretrizes da OMS para Triagem e Tratamento de Lesões Pré-cancerosas do Colo do Útero”, que recomenda o teste de DNA do HPV como o método de triagem preferido para o câncer do colo do útero.
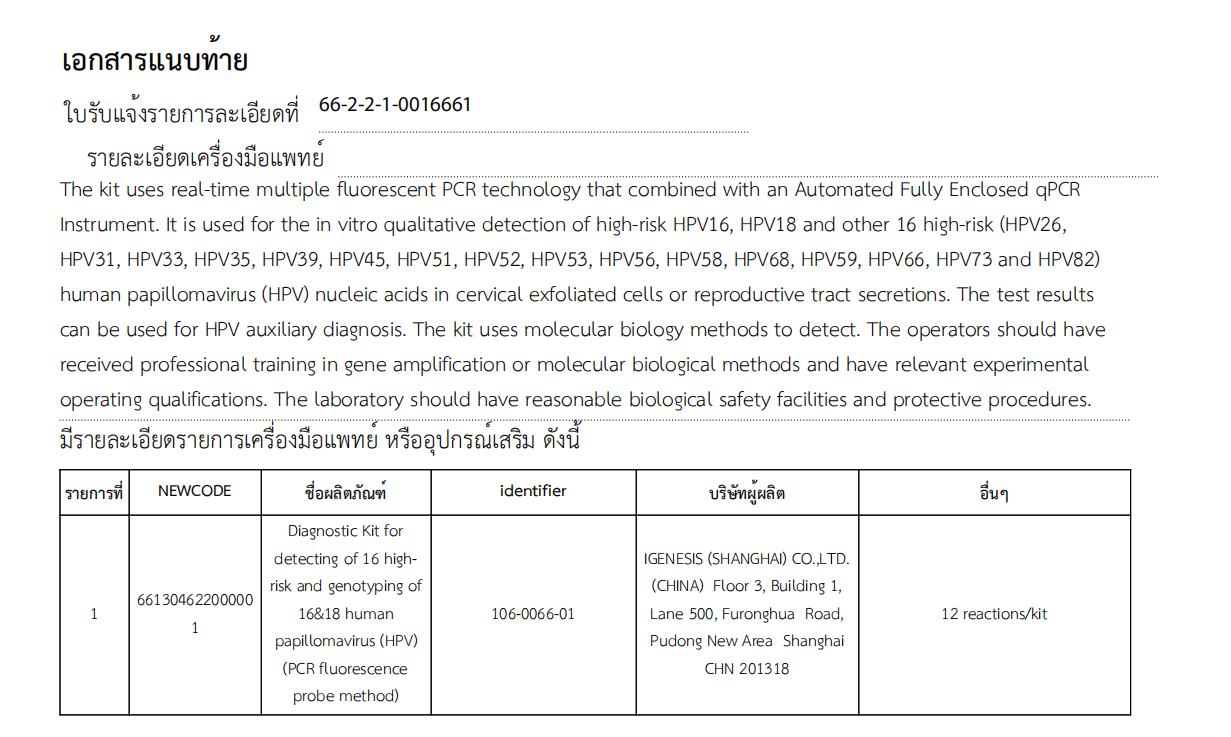
O kit de diagnóstico da Igenesis para detecção de 16 tipos de alto risco e genotipagem de 16 e 18 papilomavírus humanos (HPV) (método de sonda de fluorescência PCR) pode ser usado para detecção qualitativa de 16 tipos de alto risco (HPV16), 18 tipos de alto risco (HPV18), e outros 16 tipos de alto risco (HPV26, HPV31, HPV33, HPV35, HPV39, HPV45, HPV51, HPV52, HPV53, HPV56, HPV58, HPV68, HPV59, HPV66, HPV73 e HPV82) de papilomavírus humano in vitro a partir de células cervicais esfoliadas ou secreções genitais.Os resultados do teste podem ser usados para diagnóstico assistido por HPV, melhorar a eficiência do rastreio do cancro do colo do útero e ajudar eficazmente a prevenir e controlar o cancro do colo do útero.
O kit de detecção de ácido nucleico do HPV, quando usado em conjunto com o Galaxy Automated Fully Enclosed qPCR System, pode completar todo o processo de extração de ácido nucleico, purificação e amplificação por PCR de fluorescência em apenas 3 etapas.O processo é totalmente automático e fechado, e os resultados são precisos e confiáveis.


☑ Resultados precisos: valor CV ≤5%, taxa de coincidência é 100%;
☑ Fácil de operar: a extração de ácidos nucleicos e a análise de amplificação são totalmente automatizadas, evitando erros humanos, com boa repetibilidade de resultados, capazes de detecção de amostra única e podem ser testadas a qualquer momento;
☑ Seguro de usar: iCassette totalmente fechado, evita a poluição, garante a biossegurança
☑ Transferência de material sólido+tecnologia microfluídica;
☑ Pré-carregamento de reagente + tecnologia patenteada de liofilização;
☑ Não há necessidade de transporte de congelados.

A Igenesis se concentra na tecnologia de diagnóstico molecular em tempo real.Até outubro de 2023,igenesis obteve marca CE para 19 reagentes e instrumentos,os negócios no exterior são distribuídos globalmente, como Itália, Chile, Malásia, Espanha, Dinamarca, Hong Kong, China e Europa, América do Sul, Sudeste Asiático e outras regiões.No futuro, a igenesis continuará a explorar as infinitas possibilidades de detecção genética com a filosofia empresarial de “integridade, excelência, inovação e ganha-ganha”, e fornecer aos clientes produtos, serviços e soluções integrados de diagnóstico molecular seguros, rápidos, convenientes e precisos.
Horário da postagem: 16 de janeiro de 2024
